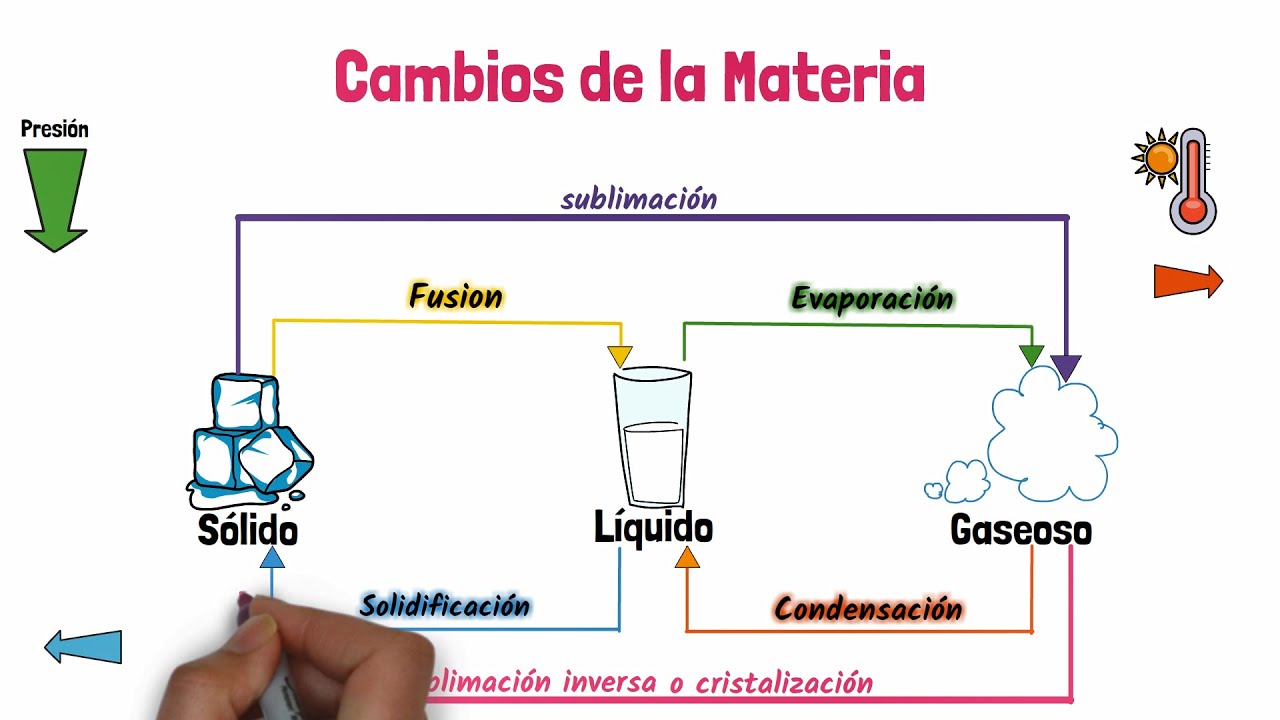
Esquema de los Cambios de Estado: Guía Completa para Entender la Materia
¿Alguna vez te has preguntado por qué el agua puede ser líquida, sólida o gaseosa? Los cambios de estado son fenómenos fascinantes que ocurren en la materia y que son fundamentales para entender cómo interactúan los diferentes elementos que nos rodean. En esta guía completa sobre el esquema de los cambios de estado, exploraremos en profundidad las transiciones entre los estados de la materia, desde la fusión hasta la sublimación. Estos procesos no solo son cruciales en la química y la física, sino que también tienen implicaciones en nuestra vida diaria, desde la forma en que cocinamos hasta cómo se forman las nubes en el cielo. Acompáñanos a desglosar cada uno de estos cambios, sus características y ejemplos prácticos que te ayudarán a entender mejor este fenómeno.
1. ¿Qué son los cambios de estado?
Los cambios de estado se refieren a las transformaciones que experimenta la materia al cambiar de un estado físico a otro. Los estados más comunes son sólido, líquido y gaseoso, y cada uno tiene propiedades distintas. El cambio entre estos estados se produce debido a la variación en la temperatura y la presión. Por ejemplo, al calentar el hielo (estado sólido), este se convierte en agua (estado líquido) y, si se sigue calentando, se transforma en vapor (estado gaseoso).
1.1 Estados de la materia
La materia puede existir en varios estados, pero los más comunes son:
- Sólido: Las partículas están muy unidas y vibran en su lugar, lo que le da forma y volumen definidos.
- Líquido: Las partículas están más separadas que en un sólido, permitiendo que fluyan y tomen la forma del recipiente que las contiene, pero con un volumen definido.
- Gas: Las partículas están muy separadas y se mueven libremente, ocupando todo el espacio disponible, sin forma ni volumen definidos.
1.2 Importancia de los cambios de estado
Comprender los cambios de estado es vital en diversas áreas como la ciencia de materiales, la meteorología y la ingeniería. Por ejemplo, en la cocina, los cambios de estado son esenciales para la preparación de alimentos, como cuando el agua hierve para cocinar pasta. En la naturaleza, estos cambios son responsables de fenómenos como la lluvia y la formación de nubes. Sin duda, los cambios de estado son un aspecto fundamental de la materia que influye en nuestro entorno y en nuestras actividades cotidianas.
2. Tipos de cambios de estado
Los cambios de estado se pueden clasificar en dos categorías principales: cambios de estado físico y cambios de estado químico. Mientras que los cambios físicos implican transformaciones en la forma o estado de la materia sin alterar su composición química, los cambios químicos resultan en la formación de nuevas sustancias. En esta sección, nos enfocaremos en los cambios de estado físico que son los más comunes y observables.
2.1 Fusión
La fusión es el proceso en el que un sólido se convierte en líquido al absorber calor. Este fenómeno ocurre a una temperatura específica conocida como punto de fusión. Por ejemplo, el hielo comienza a fundirse a 0 °C, convirtiéndose en agua líquida. Este proceso es crucial en muchos aspectos de la vida diaria, desde la fabricación de productos hasta el ciclo del agua en la naturaleza.
2.2 Vaporización
La vaporización es el cambio de estado de un líquido a gas. Este proceso puede ocurrir de dos maneras: evaporación y ebullición. La evaporación ocurre a la superficie de un líquido a cualquier temperatura, mientras que la ebullición sucede a una temperatura específica, conocida como punto de ebullición, en todo el líquido. Por ejemplo, el agua hierve a 100 °C a nivel del mar. Este proceso es fundamental en fenómenos naturales como la formación de nubes y la lluvia.
2.3 Condensación
La condensación es el proceso inverso a la vaporización, donde un gas se convierte en líquido al perder calor. Este fenómeno se observa comúnmente en la formación de gotas de agua en un vaso frío o en la niebla que se forma en las mañanas. La condensación es crucial en el ciclo del agua, donde el vapor de agua en la atmósfera se convierte en nubes y, eventualmente, en precipitación.
3. Diagramas de cambios de estado
Los diagramas de cambios de estado son herramientas visuales que representan las transiciones entre los diferentes estados de la materia. Estos diagramas son útiles para entender cómo la temperatura y la presión afectan los cambios de estado. Un ejemplo común es el diagrama de fase, que ilustra las condiciones bajo las cuales una sustancia puede existir en diferentes estados.
3.1 Diagrama de fase
El diagrama de fase muestra las áreas donde se encuentran los diferentes estados de la materia (sólido, líquido y gas) en función de la temperatura y la presión. En este diagrama, las líneas que separan las diferentes áreas representan las condiciones en las que ocurren los cambios de estado. Por ejemplo, la línea de fusión indica el punto en el que un sólido se convierte en líquido. Estos diagramas son esenciales en la química y la física para predecir el comportamiento de las sustancias bajo diferentes condiciones.
3.2 Gráficos de calentamiento y enfriamiento
Los gráficos de calentamiento y enfriamiento son otra forma de representar los cambios de estado. Estos gráficos muestran cómo la temperatura de una sustancia cambia a medida que se le añade o se le quita calor. Durante los cambios de estado, la temperatura permanece constante, lo que se refleja en el gráfico como una línea horizontal. Este tipo de representación es útil para comprender el proceso de fusión, vaporización y condensación de manera más clara.
4. Ejemplos cotidianos de cambios de estado
Los cambios de estado están presentes en nuestra vida diaria, a menudo sin que nos demos cuenta. A continuación, exploraremos algunos ejemplos cotidianos que ilustran cómo estos procesos afectan nuestro entorno y actividades.
4.1 El ciclo del agua
El ciclo del agua es un ejemplo perfecto de cómo los cambios de estado son fundamentales en la naturaleza. El agua se evapora de la superficie de océanos y ríos, formando vapor que se eleva a la atmósfera. A medida que el vapor se enfría, se condensa en nubes, y finalmente, precipita en forma de lluvia o nieve. Este ciclo es vital para la vida en la Tierra, ya que proporciona el agua necesaria para los ecosistemas y la agricultura.
4.2 Cocción de alimentos
En la cocina, los cambios de estado son cruciales para preparar alimentos. Por ejemplo, al hervir agua para cocinar pasta, el agua pasa de líquido a vapor (vaporización). Al cocinar carne, la grasa se derrite y el agua dentro de la carne se evapora, lo que transforma la textura y el sabor del alimento. Estos cambios son esenciales para la creación de platos deliciosos y nutritivos.
5. Cambios de estado en la industria
En el ámbito industrial, los cambios de estado son igualmente importantes. Se utilizan en procesos de fabricación, conservación y energía. A continuación, exploraremos cómo se aplican estos cambios en diversas industrias.
5.1 Industria alimentaria
En la industria alimentaria, los cambios de estado se utilizan en técnicas de conservación como la congelación y la deshidratación. Por ejemplo, al congelar frutas y verduras, el agua dentro de las células se convierte en hielo, lo que ayuda a preservar su frescura y nutrientes. Por otro lado, la deshidratación elimina el agua de los alimentos, prolongando su vida útil y evitando el crecimiento de bacterias.
5.2 Energía y refrigeración
Los cambios de estado son fundamentales en sistemas de refrigeración y generación de energía. En los refrigeradores, el refrigerante se evapora y condensa, permitiendo que el calor se extraiga del interior del aparato. Asimismo, en las plantas de energía, el agua se calienta para convertirse en vapor, que luego impulsa turbinas para generar electricidad. Estos procesos son esenciales para la eficiencia energética y el confort en nuestros hogares.
6. Preguntas Frecuentes (FAQ)
¿Qué es un cambio de estado?
Un cambio de estado es la transformación de una sustancia de un estado físico a otro, como sólido, líquido o gas. Esto ocurre debido a variaciones en la temperatura y la presión, afectando la energía de las partículas que componen la materia.
¿Cuáles son los cambios de estado más comunes?
Los cambios de estado más comunes son la fusión (sólido a líquido), la vaporización (líquido a gas), la condensación (gas a líquido) y la solidificación (líquido a sólido). Cada uno de estos procesos tiene características y condiciones específicas bajo las cuales ocurre.
¿Qué es el punto de fusión?
El punto de fusión es la temperatura a la cual un sólido se convierte en líquido. Cada sustancia tiene un punto de fusión específico; por ejemplo, el hielo se funde a 0 °C. Este concepto es fundamental para entender los cambios de estado en la materia.
¿Cómo afecta la presión a los cambios de estado?
La presión puede influir significativamente en los cambios de estado. Por ejemplo, al aumentar la presión, el punto de ebullición de un líquido puede aumentar, lo que significa que se necesitará más calor para que el líquido se convierta en vapor. Esto es especialmente relevante en aplicaciones industriales y científicas.
¿Qué es la sublimación?
La sublimación es un cambio de estado en el que una sustancia pasa directamente de sólido a gas sin pasar por el estado líquido. Un ejemplo común es el hielo seco (dióxido de carbono sólido), que se sublima a temperatura ambiente, produciendo vapor de gas.
¿Por qué es importante entender los cambios de estado?
Comprender los cambios de estado es esencial en diversas áreas como la ciencia, la industria y la vida cotidiana. Estos procesos son fundamentales para la fabricación de productos, la conservación de alimentos y el funcionamiento de sistemas energéticos, entre otros. Además, nos ayudan a entender fenómenos naturales como el ciclo del agua.
¿Cuáles son algunas aplicaciones prácticas de los cambios de estado?
Las aplicaciones prácticas de los cambios de estado son numerosas e incluyen la cocina, la conservación de alimentos, la refrigeración, la generación de energía y la meteorología. Cada uno de estos campos utiliza los principios de los cambios de estado para mejorar la calidad de vida y optimizar procesos industriales.